オキサリプラチン点滴静注液「DSEP」
医療関係者向け資材
対象の資材はありません
患者さん向け資材
弊社の患者指導用資材をご紹介しております。
ご入用の場合は、資材お取り寄せサービスをご利用いただくか、弊社医薬情報担当者(MR)にお申し付けください。
資材お取り寄せについて
STEP1
資材を選択
STEP2
お届け先情報を入力
STEP3
資材をお届け
- ・お届け先は、医療機関に限らせていただきます。
- ・ご請求いただいてから、通常2〜3営業日、最大7営業日程度でお届けいたします。
- ・在庫がない場合、1〜2週間程度お時間をいただくことがございます。できる限り早くお届けできるよう努めておりますが、 天候不順・道路交通網の混雑などにより、遅れが生じる場合がございます。
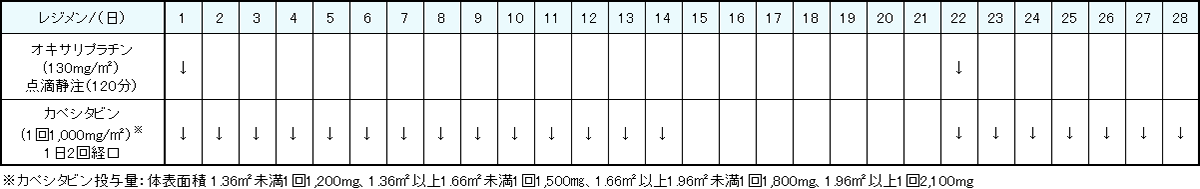
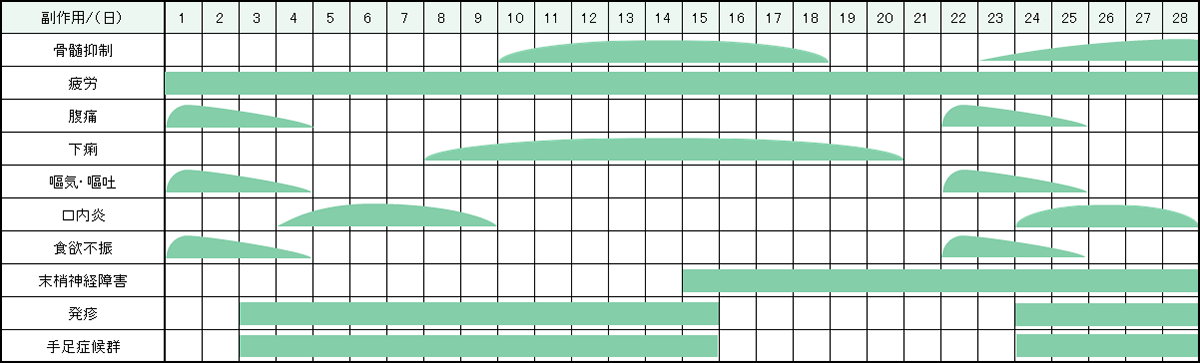
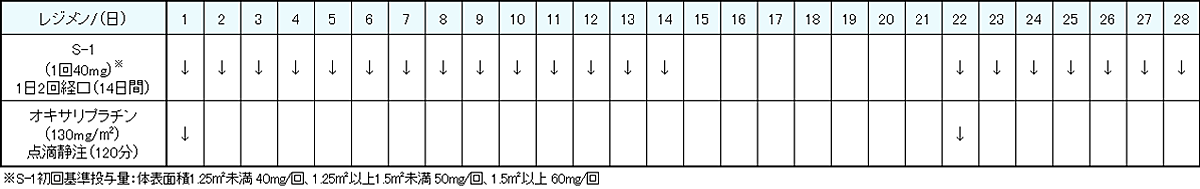
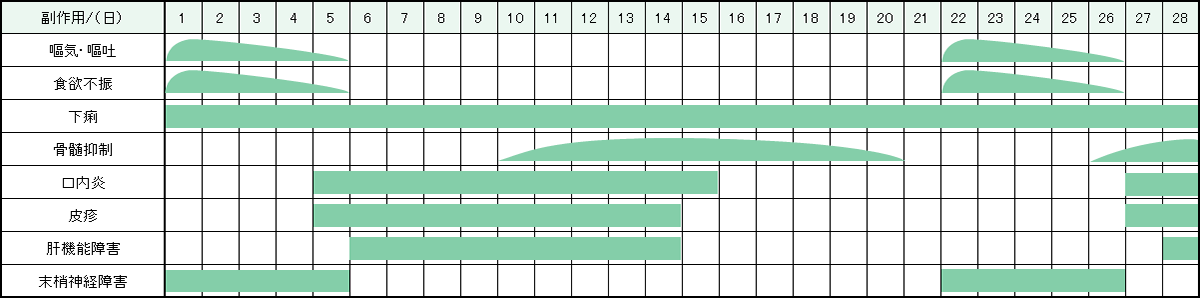
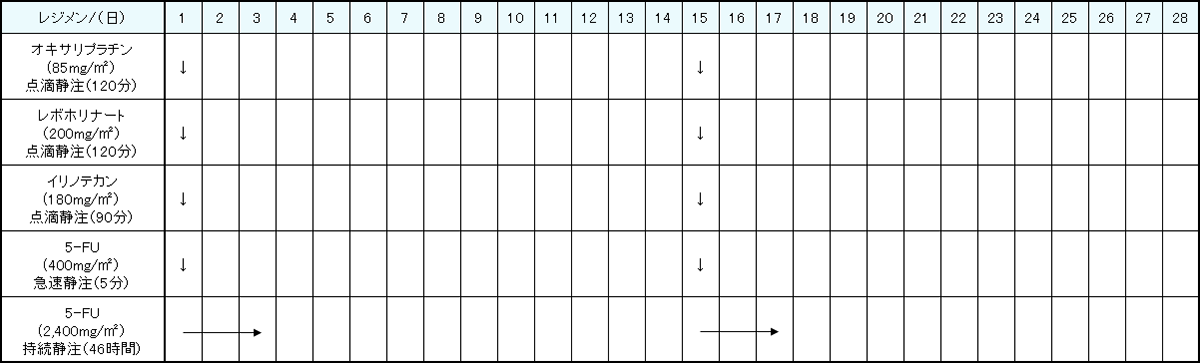
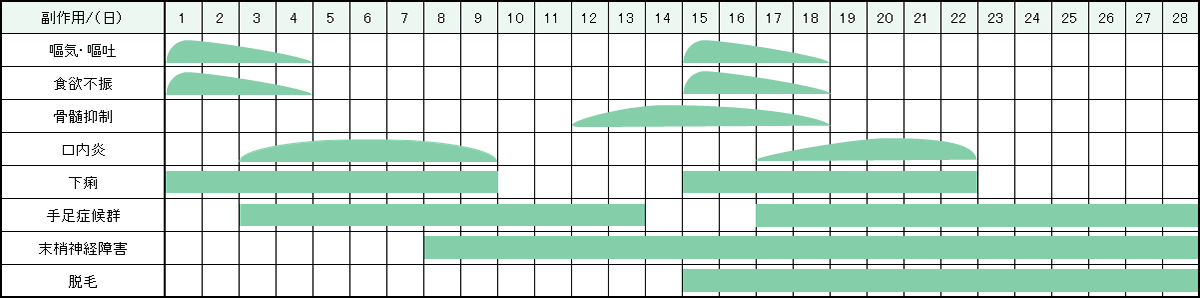
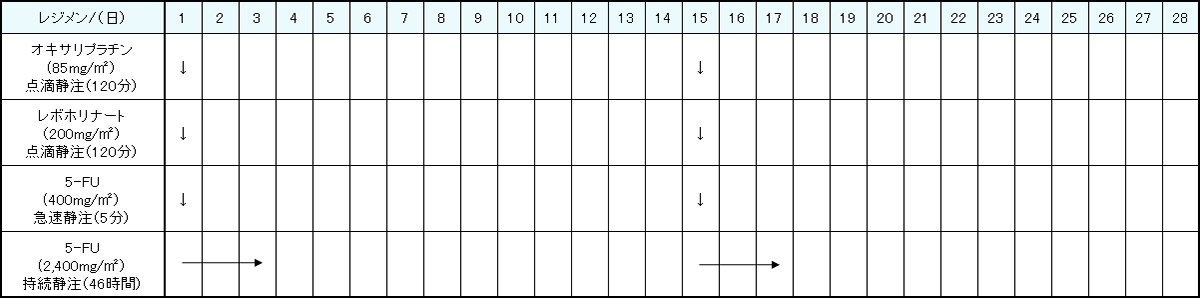
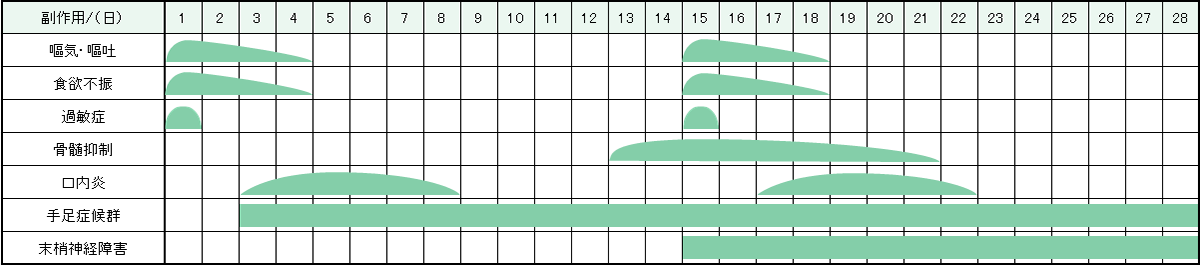
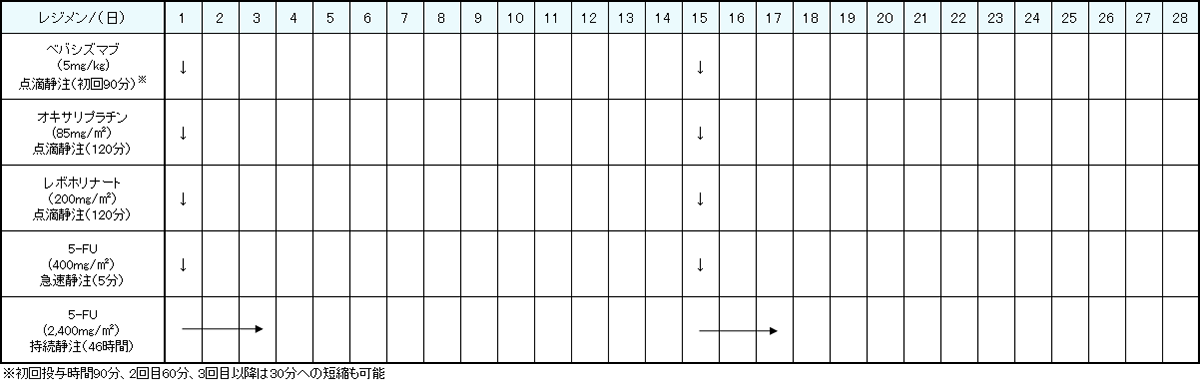
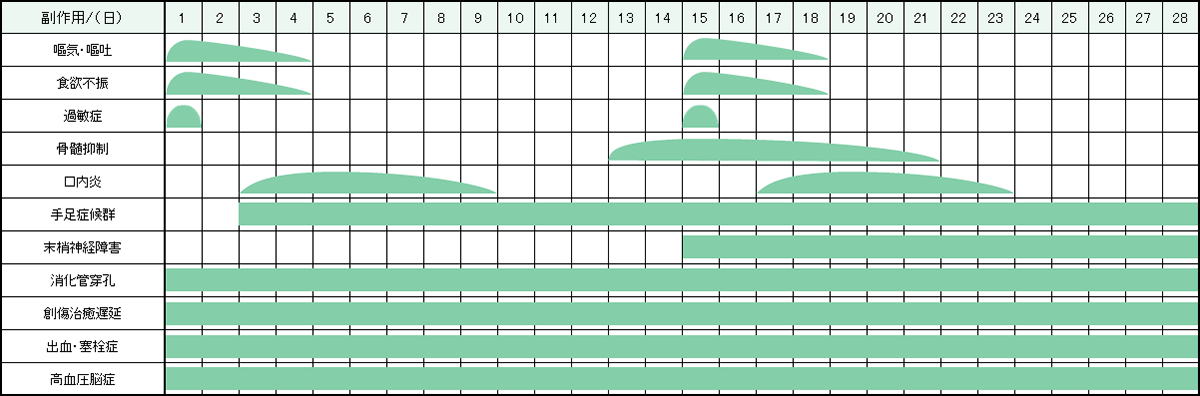
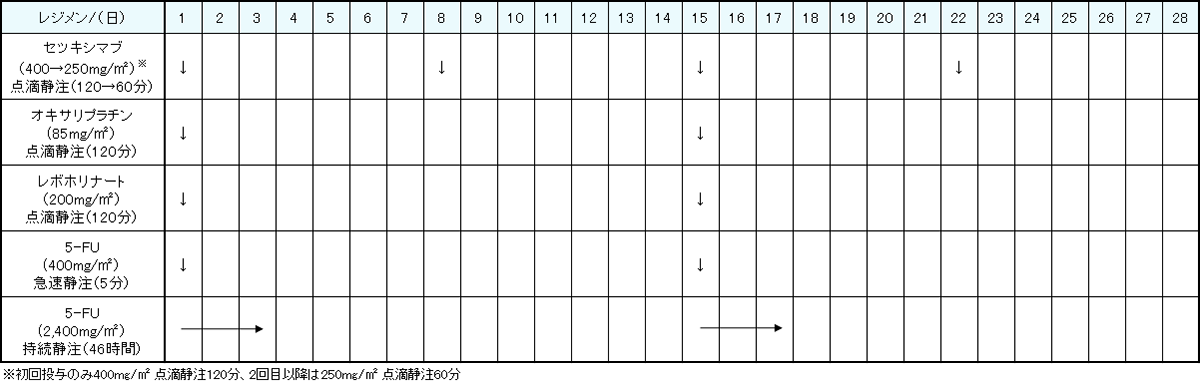
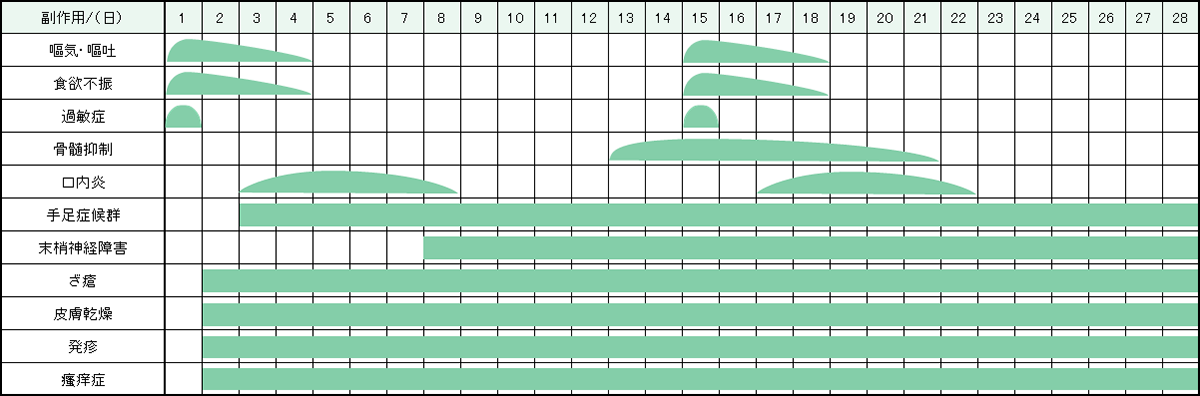
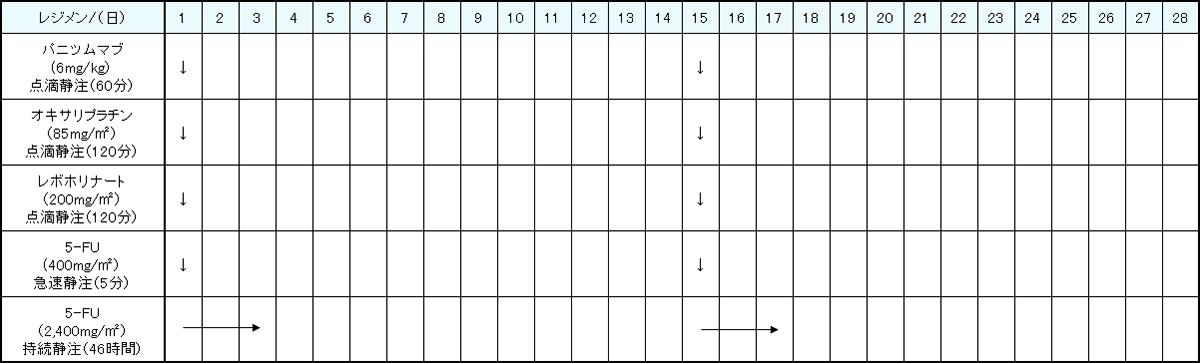
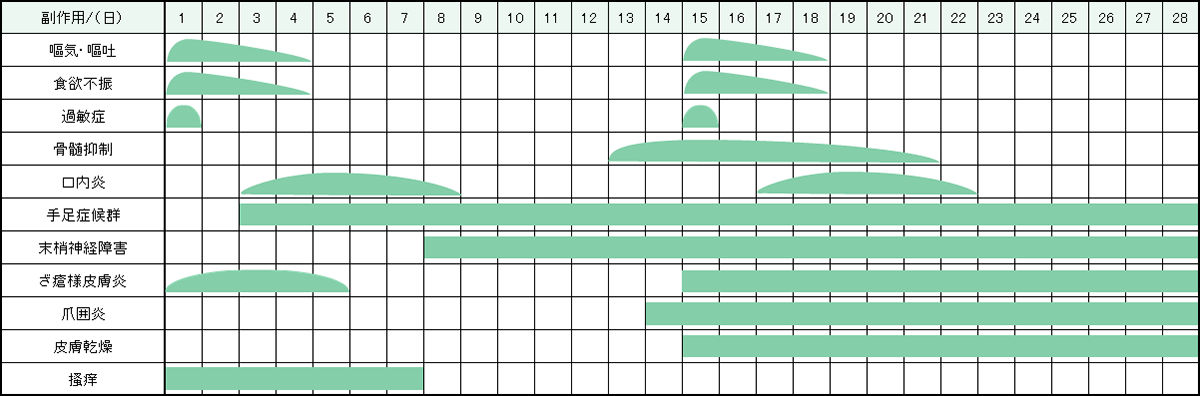
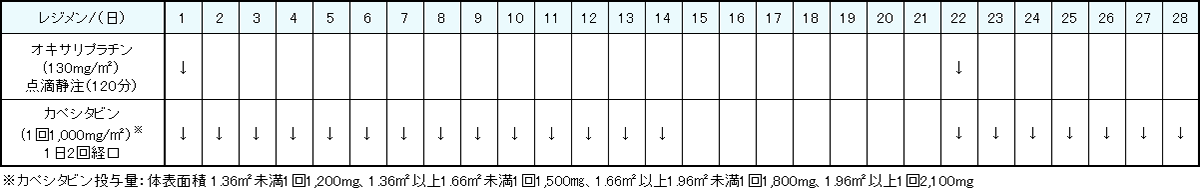
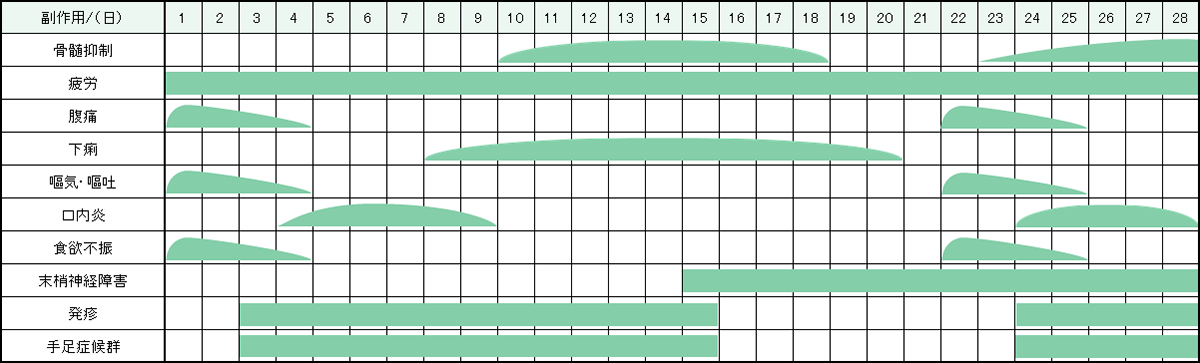
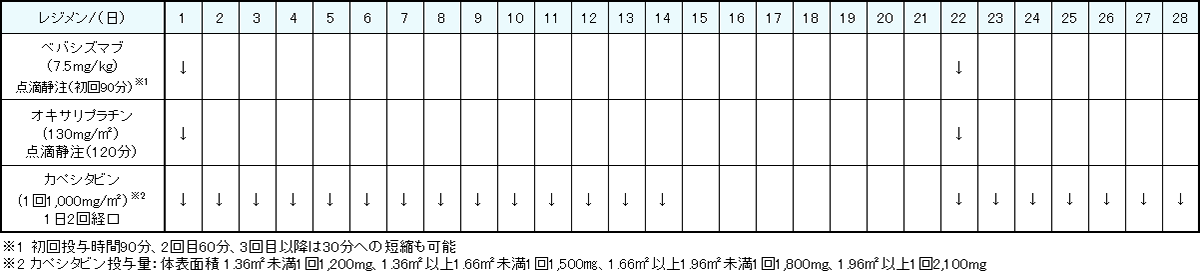
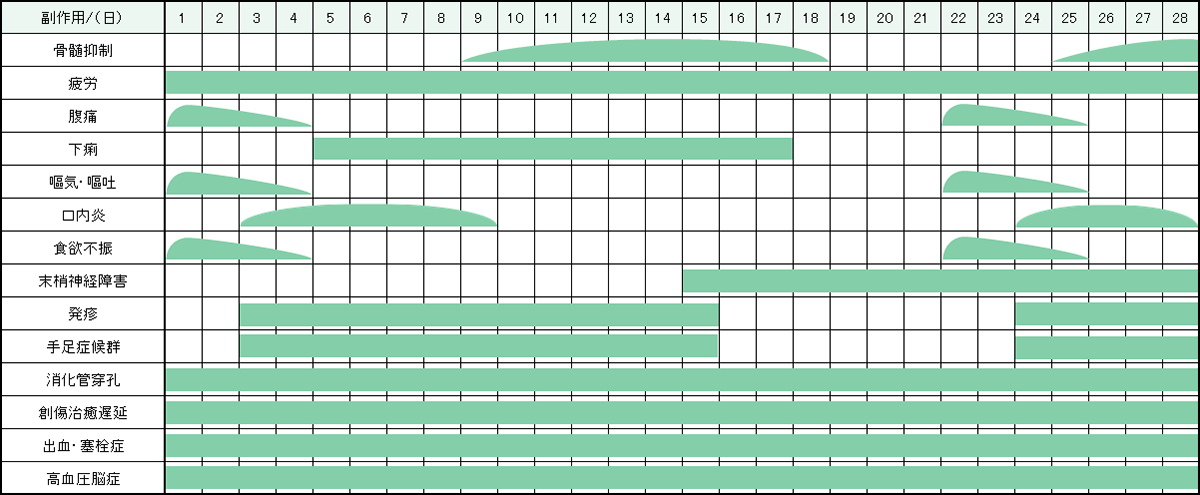
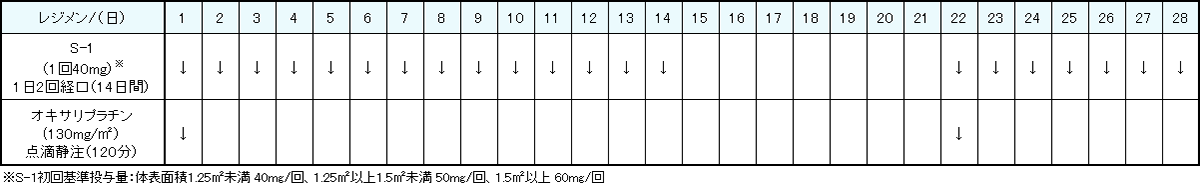
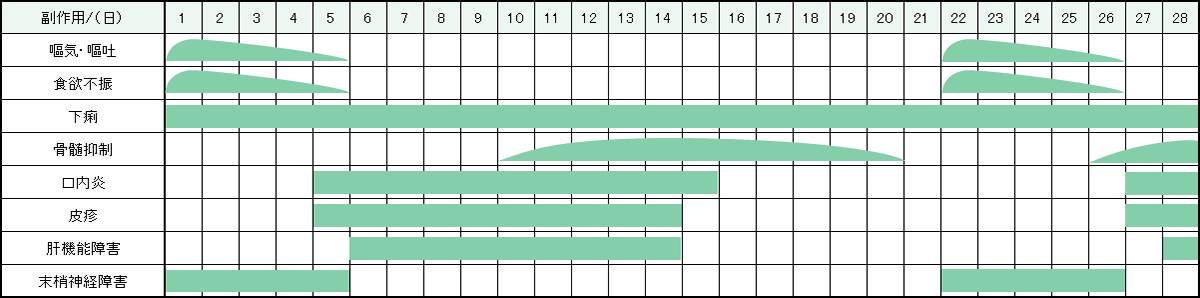
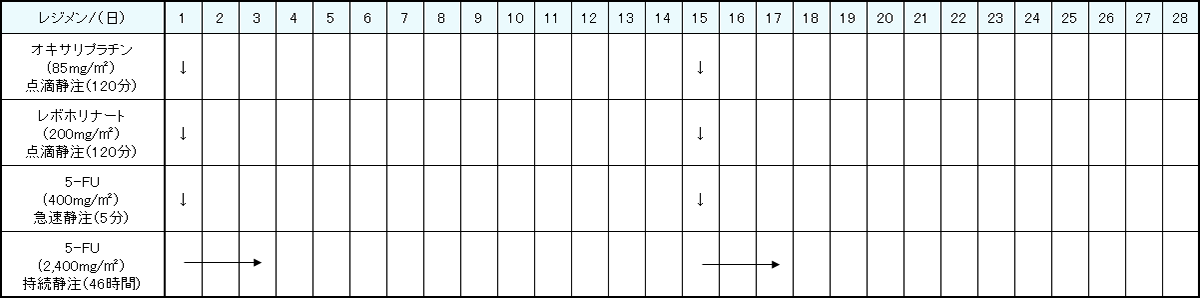
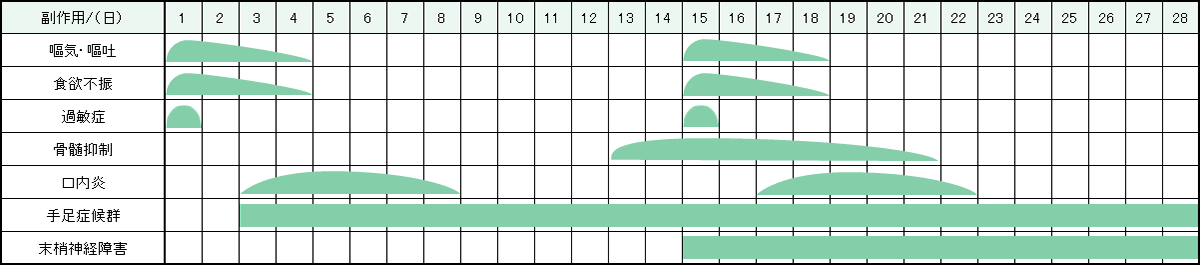
レジメン・副作用情報
- 胃がん
- 膵がん
- 大腸がん
- 小腸がん
2023年10月現在の情報となります。
参考書籍:改訂版 がん化学療法副作用対策ハンドブック(羊土社)
改訂第5版がん化学療法レジメンハンドブック(羊土社)
監修:医療法人社団 千葉ポートメディカルクリニック 今村 貴樹 先生
製品のお知らせ
2026.04.16
販売中止・休止
販売終了製品のご案内(オキサリプラチン点滴静注液、オランザピン錠・OD錠・細粒、カンデサルタン錠、ブロナンセリン錠、レバミピド錠)
2025.12.26
包装変更
25年12月 添付文書の同梱終了品 出荷予定時期一覧のご案内【更新:販売終了製品・販売終了時期】(電子添文化対応)
2025.04.15
包装・表示変更
オキサリプラチン点滴静注液「DSEP」日本薬局方収載に伴う表示変更のご案内
2023.08.30
安全性情報
オキサリプラチン点滴静注液50mg・点滴静注液100mg・点滴静注液200mg「DSEP」効能又は効果/用法及び用量/使用上の注意改訂のお知らせ
2023.08.30
製品
オキサリプラチン点滴静注液「DSEP」効能又は効果、用法及び用量一部変更のご案内
2020.01.14
安全性情報
オキサリプラチン点滴静注液50mg/100mg/200mg「DSEP」使用上の注意改訂のお知らせ
2019.01.15
安全性情報
オキサリプラチン点滴静注液50mg/100mg/200mg「DSEP」使用上の注意改訂のお知らせ
2018.09.21
効能・効果等追加
オキサリプラチン点滴静注液50mg/100mg/200mg「DSEP」効能・効果、用法・用量追加のご案内
2018.09.21
安全性情報
オキサリプラチン点滴静注液50mg/100mg/200mg「DSEP」効能・効果、用法・用量、使用上の注意改訂のお知らせ
2016.10.24
安全性情報
オキサリプラチン点滴静注液50mg「DSEP」、100mg「DSEP」、200mg「DSEP」使用上の注意改訂のお知らせ
2016.08.03
安全性情報
オキサリプラチン点滴静注液50mg/100mg/200mg「DSEP」取扱い上の注意改訂のお知らせ
2016.05.23
製品
オキサリプラチン「DSEP」のくすりのしおりを変更しました
2016.04.27
効能・効果等追加
オキサリプラチン点滴静注液50mg/100mg/200mg「DSEP」効能・効果、用法・用量追加のご案内
2016.04.27
安全性情報
オキサリプラチン点滴静注液「DSEP」効能・効果_用法・用量_使用上の注意改訂のお知らせ
2016.01.20
安全性情報
オキサリプラチン「DSEP」取扱い上の注意改訂のお知らせ
2015.08.18
製品
くすりのしおりを掲載しました(和文・英文:オキサリプラチン点滴静注液「DSEP」)。
2015.08.05
安全性情報
オキサリプラチン点滴静注液「DSEP」効能・効果_用法・用量_使用上の注意改訂のお知らせ
2015.07.09
製品
くすりのしおりを掲載しました(和文・英文:ナフトピジルOD錠25/50/75mg「DSEP」、メトホルミン塩酸塩錠250/500mgMT「DSEP」、レトロゾール錠2.5mg「DSEP」、オキサリプラチン点滴静注液200mg「DSEP」)。
2015.06.19
新発売
新発売のご案内 オキサリプラチン点滴静注液200mg「DSEP」
2015.02.16
製造販売承認取得
製造販売承認取得のご案内(ナフトピジル、メトホルミン、レトロゾール、オキサリプラチン)
2014.12.26
製品
くすりのしおりを更新しました(オキサリプラチン点滴静注液50mg「DSEP」、オキサリプラチン点滴静注液100mg「DSEP」)。
2014.12.24
効能・効果等追加
オキサリプラチン点滴静注液50mg/100mg「DSEP」効能・効果、用法・用量追加のご案内
2014.12.24
安全性情報
オキサリプラチン点滴静注液50mg「DSEP」、液100mg「DSEP」効能・効果/用法・用量/使用上の注意改訂のお知らせ
2014.12.12
製品
くすりのしおりを掲載しました(レボフロキサシン錠・細粒「DSEP」、オキサリプラチン点滴静注液「DSEP」、エペリゾン塩酸塩錠50mg「日新」、カンデサルタン錠「DSEP」)。
2014.12.12
新発売
新発売のご案内(オキサリプラチン点滴静注液50mg/100mg「DSEP」)
2014.10.18
製品
2014年8月承認取得製品(オキサリプラチン点滴静注液50mg「DSEP」、液100mg「DSEP」、カンデサルタン錠2mg「DSEP」、錠4mg「DSEP」、錠8mg「DSEP」、錠12mg「DSEP」、レボフロキサシン錠250mg「DSEP」、錠500mg「DSEP」、細粒10%「DSEP」)の情報を公開しました
2014.09.01
製造販売承認取得
製造販売承認取得のご案内(レボフロキサシン錠/細粒、カンデサルタン錠、オキサリプラチン点滴静注液)
2014.09.01
新発売予定
2014年12月近日発売製品のご案内(レボフロキサシン錠/細粒「DSEP」、カンデサルタン錠「DSEP」、オキサリプラチン点滴静注液「DSEP」)